اتم های عناصر مختلف دارای الکترونهایی هستند که در مدارهای مختلفی به دور هسته گردش می کنند . الکترونهایی که در مدارهای نزدیک به هسته گردش می کنند انرژی کمتری دارند اما از طرف هسته ، نیروی جاذبه بیشتری بر آنها وارد می شود و در نتیجه نمی توان به آسانی این الکترونها را از اتم جدا کرد .
در هر اتم ، آخرین مدار را لایه ظرفیت یا لایه والانس می گویند و الکترونهای این لایه را الکترونهای ظرفیت یا والانس می نامند . الکترونهای والانس انرژی بیشتری نسبت به بقیه الکترونها دارند اما وابستگی آنها به هسته کمتر از بقیه الکترونها می باشد . در شکل (1) ساختمان اتمی اتم مس نمایش داده شده است . همانطور که در این شکل مشاهده می کنید اتم مس فقط یک الکترون والانس دارد .
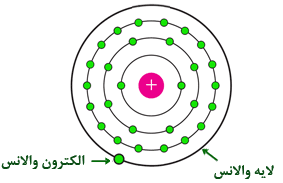
شکل (1)
اجسام موجود در طبیعت بر اساس تعداد الکترونهای والانس اتم های تشکیل دهنده آنها به سه دسته اجسام هادی ، اجسام عایق و اجسام نیمه هادی تقسیم می شوند که در ادامه به بررسی آنها می پردازیم .
اجسام هادی : اتم های تشکیل دهنده این اجسام کمتر از چهار الکترون والانس دارند و این الکترونها به راحتی از قید هسته آزاد می شوند . اجسام هادی الکترونهای آزاد زیادی دارند و این الکترونهای آزاد سبب عبور جریان برق می شوند . به این اجسام رسانا هم می گویند . فلزات یک تا سه ظرفیتی هادی های خوبی هستند و بهترین هادی ها عبارتند از : نقره ، مس و طلا .
اجسام عایق : اتم های تشکیل دهنده این اجسام معمولاً دارای پنج تا هشت الکترون والانس هستند . به علت اینکه انرژی داده شده به اتم های اجسام عایق میان تعداد زیادی الکترون والانس تقسیم می شود انرژی دریافت شده توسط هر الکترون بسیار ناچیز است و بنابراین این الکترونها به سختی از اتم جدا می شوند و همین امر سبب می شود که اجسام عایق در وضعیت معمولی دارای الکترونهای آزاد بسیار کمی بوده و جریان برق را از خود عبور ندهند .
اجسام نیمه هادی : اتم های تشکیل دهنده اجسام نیمه هادی معمولاً دارای چهار الکترون والانس می باشند . اجسام نیمه هادی در دمای صفر مطلق ( 273– درجه سانتیگراد ) تقریباً عایق هستند . در دمای اتاق ( 25 درجه سانتیگراد ) ، انرژی حرارتی محیط باعث آزاد شدن تعدادی از الکترونهای والانس می شود و هدایت الکتریکی در جسم بالا می رود . در دمای اتاق ، هدایت الکتریکی نیمه هادی ها بهتر از عایق ها و بدتر از هادی ها می باشد . نیمه هادی های پرکاربرد عبارتند از کربن ، سیلیسیم ( سیلیکن ) ، ژرمانیوم ، توریم ، زیرکونیوم و هافنیوم که از بین آنها سیلیسیم و ژرمانیوم در برق و الکترونیک کاربرد فراوان دارند . در ادامه به بررسی نیمه هادی های سیلیسیم و ژرمانیوم می پردازیم .
سیلیسیم دارای عدد اتمی 14است . یعنی دارای 14 پروتون و 14 الکترون است . ژرمانیوم دارای عدد اتمی 32 است . یعنی 32 پروتون و 32 الکترون دارد . در شکل (2) ساختمان اتمی سیلیسیم و در شکل (3) ساختمان اتمی ژرمانیوم نمایش داده شده است . همانطور که در این شکل ها مشاهده می کنید هر یک از اتم های سیلیسیم و ژرمانیوم دارای چهار الکترون والانس هستند .

شکل (2)

شکل (3)
به علت اینکه سیلیسیم و ژرمانیوم در مدار آخر خود چهار الکترون دارند ، تمایل دارند که مدار آخر خود را کامل کرده و به حالت پایدار برسند . برای این منظور هر اتم با هر یک از چهار اتم مجاور خود یک الکترون به اشتراک می گذارد . این نوع پیوند بین اتم ها را پیوند اشتراکی یا کووالانسی می گویند . در شکل (4) پیوندهای کووالانسی بین اتم های سیلیسیم نمایش داده شده است .

شکل (4)
در یک بلور سیلیسیم یا ژرمانیوم ، در دمای صفر مطلق به علت اینکه تمامی پیوندهای کووالانسی بین اتم ها برقرار است و هیچ الکترون آزادی وجود ندارد بلور سیلیسیم یا ژرمانیوم یک عایق کامل می باشد . اما با افزایش دما جنبش الکترونهای والانس افزایش یافته و بعضی از پیوندهای کووالانسی بین اتم ها شکسته شده و الکترونهایی آزاد می شوند و به این ترتیب هدایت الکتریکی در کریستال های سیلیسیم و ژرمانیوم افزایش می یابد . هر چه دما بیشتر افزایش یابد پیوندهای کووالانسی بیشتری شکسته شده و تعداد الکترونهای آزاد بیشتر می شود و در نتیجه هدایت الکتریکی کریستال افزایش می یابد . به ازای جدا شدن هر الکترون از یک اتم ، یک جای خالی الکترون در آن اتم ایجاد می شود که به آن حفره می گویند . در شکل (5) نحوه ایجاد یک حفره نمایش داده شده است .

شکل (5)
الکترونهای آزاد شده در کریستال به صورت نامنظم حرکت می کنند . اگر به صورت اتفاقی الکترونی به حفره ای نزدیک شود جذب حفره می گردد . بنابراین تا زمانی که نیرویی از خارج بر کریستال اعمال نشود آزاد شدن الکترونها و جذب آنها به وسیله حفره ها به طور نامنظم ادامه می یابد . اما زمانی که ولتاژی به دو سر کریستال اعمال می شود ، الکترونهای آزاد به طرف قطب مثبت باتری حرکت می کنند و جریانی در کریستال اعمال می شود که ناشی از حرکت الکترونهاست و به آن جریان الکترونها می گویند . جریان دیگری نیز در کریستال وجود دارد که ناشی از حرکت حفره هاست . اگر در اتمی حفره ای وجود داشته باشد این حفره از اتم مجاور ، الکترونی را جذب می کند . اما جای الکترون جذب شده ، حفره جدیدی ایجاد می گردد و با اینکه حفره ها حرکت نمی کنند اما به نظر می رسد که آنها در حال حرکت هستند . به این ترتیب وقتی الکترونی مثلاً از راست به چپ حرکت می کند به نظر می رسد که حفره از چپ به راست در حرکت است . دقت داشته باشید که همواره جهت حرکت فرضی حفره ها در خلاف جهت حرکت الکترونها می باشد .
چون تعداد الکترونهای آزاد و حفره های ایجاد شده در کریستال های سیلیسیم و ژرمانیوم در اثر انرژی گرمایی به اندازه کافی زیاد نیست این کریستال ها قابلیت هدایت الکتریکی خوبی ندارند . برای افزایش قابلیت هدایت الکتریکی این نیمه هادی ها به آنها ناخالصی اضافه می کنند . اضافه کردن ناخالصی به نیمه هادی ها به دو شکل صورت می گیرد .
1- ناخالص کردن کریستال نیمه هادی با اتم پنج ظرفیتی
2- ناخالص کردن کریستال نیمه هادی با اتم سه ظرفیتی
ناخالص کردن کریستال نیمه هادی با اتم پنج ظرفیتی : در این روش عناصر پنج ظرفیتی مانند آرسنیک (As) ، آنتیموان (Sb) و یا فسفر (P) را که در لایه ظرفیت خود پنج الکترون دارند به کریستال سیلیسیم یا ژرمانیوم اضافه می کنند . به عنوان مثال در شکل (6) عنصر پنج ظرفیتی آرسنیک به کریستال سیلیسیم اضافه شده است .

شکل (6)
همانطور که در شکل (6) مشاهده می کنید اتم ناخالصی آرسنیک با چهار اتم سیلیسیم مجاور خود تشکیل پیوند اشتراکی می دهد و چون در لایه ظرفیت اتم آرسنیک فقط جای 8 الکترون وجود دارد یک الکترون اتم ناخالصی به راحتی از قید هسته آزاد می گردد و به صورت الکترون آزاد درمی آید . پس با افزودن هر اتم ناخالصی ، یک الکترون آزاد به وجود می آید . با تنظیم مقدار اتم ناخالصی ، تعداد الکترونهای آزاد کریستال را کنترل می کنند . علاوه بر الکترونهای آزادی که از افزودن اتم ناخالصی در کریستال به وجود می آیند تعداد کمی الکترون نیز در اثر انرژی گرمایی محیط از قید هسته آزاد می شوند و جای خالی آنها حفره ایجاد می گردد . اتم ناخالصی که به کریستال یک الکترون آزاد می دهد و خود به صورت یون مثبت درمی آید اتم اهدا کننده نام دارد . چون در این کریستال ها تعداد الکترونهای آزاد که عمل هدایت الکتریکی را انجام می دهند به مراتب بیشتر از تعداد حفره ها است به الکترونهای آزاد ، حامل های اکثریت و به حفره ها ، حامل های اقلیت می گویند . این نوع کریستال ها را که حامل های اکثریت آنها الکترون ها هستند کریستال های نوع N می نامند که N از کلمه Negative به معنی منفی گرفته شده است . زیرا در این نوع کریستال ها بار حامل های اکثریت یعنی الکترونها منفی است . البته کل کریستال از نظر بار الکتریکی خنثی است زیرا بارهای مثبت و منفی آن با هم برابرند . در شکل (7) تصویری نمادین از حامل های اکثریت و اقلیت در نیمه هادی نوع N نمایش داده شده است . در این شکل دایره های سفید رنگ ، بیانگر حفره و دایره های قرمز رنگ دنباله دار ، بیانگر الکترونهای آزاد در حال حرکت هستند .

شکل (7)
ناخالص کردن کریستال نیمه هادی با اتم سه ظرفیتی : هرگاه یک عنصر سه ظرفیتی مانند آلومینیوم (Al) ، گالیم (Ga) و یا ایندیم (In) را که در مدار ظرفیت خود سه الکترون دارند به کریستال سیلیسیم یا ژرمانیوم خالص اضافه کنیم الکترونهای مدار آخر عنصر ناخالصی مانند آلومینیوم با الکترونهای والانس اتم های مجاور خود تشکیل پیوند کووالانسی می دهند . به این ترتیب در مدار آخر اتم ناخالصی هفت الکترون در حال گردش هستند که در نتیجه یک جای خالی یا حفره ایجاد می شود . در شکل (7) اضافه کردن اتم ناخالصی آلومینیوم به کریستال سیلیسیم نمایش داده شده است .
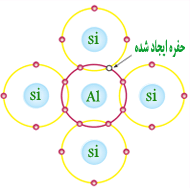
شکل (8)
همانطور که در شکل (8) مشاهده می کنید با افزودن یک اتم سه ظرفیتی به یک کریستال نیمه هادی یک حفره ایجاد می شود . ممکن است الکترونی در اثر داشتن انرژی جنبشی کافی ، پیوند خود با الکترون دیگر را شکسته و محل این حفره را پر نماید که در این صورت حفره جدیدی در کریستال ایجاد می شود . بنابراین به ازای اضافه کردن هر اتم سه ظرفیتی به یک نیمه هادی ، مطمئناً یک حفره در آن نیمه هادی ایجاد می شود . به اتم سه ظرفیتی که قادر است یک الکترون آزاد را جذب کند اتم پذیرنده گویند . اتم پذیرنده با دریافت الکترون به صورت یون منفی درمی آید . در اثر گرمای محیط تعداد کمی الکترون نیز انرژی لازم را کسب می کنند و از هسته خود جدا می شوند و به صورت الکترون آزاد درمی آیند . بنابراین در کریستال علاوه بر تعداد زیادی حفره که حامل های اکثریت هستند ، تعداد اندکی الکترون آزاد یعنی حامل های اقلیت نیز وجود دارند . چون در این نوع کریستال ها ، حفره ها که دارای بار مثبت هستند حامل های اکثریت هستند این نوع کریستال ها را ، کریستال های نوع P می نامند که P از کلمه Positive به معنای مثبت گرفته شده است . در شکل (9) تصویری نمادین از حامل های اکثریت و اقلیت در نیمه هادی نوع P نمایش داده شده است .

شکل (9)
 hamed - مهدی جان اولین سالگرد سایتت تبریک میگم
hamed - مهدی جان اولین سالگرد سایتت تبریک میگم پرهام - مرسی
پرهام - مرسی  علي -
علي -  آبی - چرا ضمیمه های جدید رو نمیذاری
آبی - چرا ضمیمه های جدید رو نمیذاری آبی -
آبی - ![]()
 احمد - سلام وبسایت خوبی داری خوشم اومد مطالبت به روزه من هرروز بهت سر میزنم قربانت احمد
احمد - سلام وبسایت خوبی داری خوشم اومد مطالبت به روزه من هرروز بهت سر میزنم قربانت احمد رهـــــــــــا - سلام
رهـــــــــــا - سلام




.JPG)

.jpeg)

















